기존 항암제가 해결하지 못한 암 재발의 문제를 극복해 줄 암 치료 원리가 제시되었다.
충북대 배석철 교수 연구팀이 암세포가 자살을 결정하지 않고 생존을 이어가는 핵심원리를 제시했다고 한국연구재단이 4월 30일 밝혔다.
한번 암이 발병했던 환자는 항암치료를 통해 종양을 제거하더라도 다른 유전자가 변이되면서 항암제가 듣지 않는 암으로 재발한다. 표적치료를 비롯해 과거보다 우수한 항암제가 다수 개발되었음에도 불구하고, 암의 재발은 아직도 해결되지 않았다.
기존 연구들은 암 억제 유전자인 ‘p53'의 기능이 파괴되기 때문에 암이 재발한다고 설명했다. 그러나 최근 연구에서는 p53의 기능이 복구되어도 이미 발병한 암은 치료되지 않음이 밝혀졌다. 이에 재발과정에 대한 새로운 패러다임의 정립이 필요해졌다.
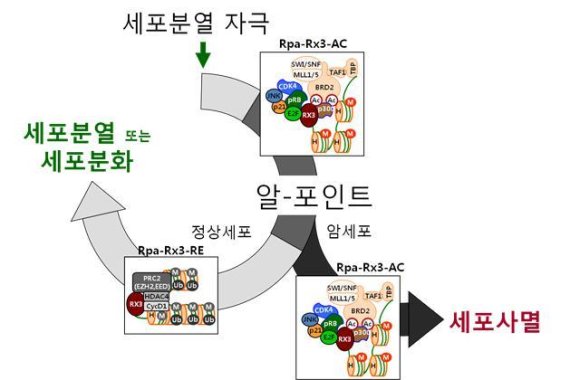
연구팀은 암세포의 비정상적인 세포분열 과정에 주목했다. 세포가 생명을 지속하거나 사멸하도록 스스로 결정하는 절차인 ‘R-포인트(Restriction point)'의 진행과정을 유전자 수준에서 규명해, 암의 재발을 막을 방법을 구했다.
특히 암세포에서 R-포인트가 붕괴되는 주요원인은 'Runx3'이라는 유전자 기능이 저하되기 때문을 밝혀냈다. 암세포에 Runx3를 도입하면 암세포의 자살 결정과정을 원상 복구시킴으로써 암세포만 선별적으로 사멸시킬 수 있다.
배석철 교수는 “R-포인트는 암세포 자살을 유도하므로, 이론적으로 암세포의 효과적 제거 뿐 아니라 다른 암유전자의 2차적 활성도 차단할 수 있을 것으로 기대한다”고 연구의의를 설명하며, “향후 이 원리를 적용해 재발없는 항암제 개발 연구를 진행할 계획”이라고 후속 연구계획을 밝혔다.
이 연구 성과는 과학기술정보통신부·한국연구재단 기초연구사업(리더연구)의 지원으로 수행되었다. 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 4월 23일 게재되었다.
seokjang@fnnews.com 조석장 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지