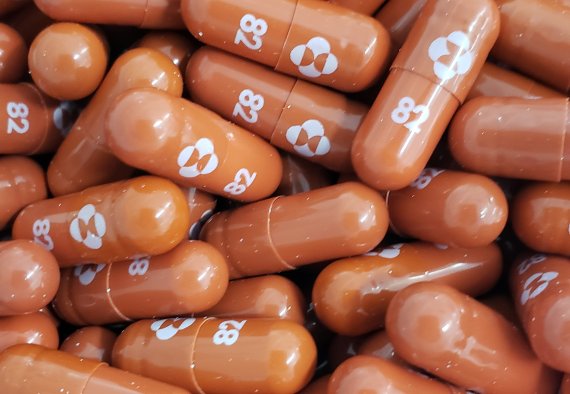
(서울=뉴스1) 최서윤 기자 = 미국 식품의약국(FDA)이 머크(Merck, MSD)의 알약형 코로나19 치료제 '몰누피라비르' 승인 여부를 11월 30일 논의한다고 14일(현지시간) 밝혔다.
머크는 지난 11일 FDA에 몰누피라비르 긴급사용승인을 신청했다. 승인이 이뤄질 경우 최초의 먹는 코로나19 항체 치료제가 출시되는 셈으로, 미국에선 연내 사용도 가능할 전망이다.
로이터 통신에 따르면 FDA 외부 전문가 패널(토론자)은 경증 코로나 감염자 가운데 중증 진행 가능성이 큰 성인 환자 치료에 있어 몰누피라비르의 효과와 안전성을 검토하는 회의를 11월30일 개최한다.
다만, FDA가 일반적으로 전문가 패널의 권고를 따르긴 해도, 반드시 그래야 할 의무는 없다.
또 FDA의 결정이 이뤄져도, 미 질병통제예방센터(CDC)의 사용 권고 논의 절차가 남아있다.
머크의 몰누피라비르는 정맥 주사 형태의 기존 항체치료제 '렘데시비르'와 달리, 알약 형태로 복용이 쉬워, 백신과 함께 '위드 코로나(코로나 일상)'의 핵심 수단으로 주목받고 있다.
화이자 이사를 맡고 있는 스콧 고틀립 전 FDA 국장은 최근 인터뷰에서 "머크의 연구 결과는 지금껏 나온 호흡기 병원체 치료 관련 경구용 항바이러스제 중 최고의 치료 효과를 보여준다"며 "몰누피라비르가 출시되면 중대한 변화를 가져올 수 있다"고 평가한 바 있다.
앞서 머크는 올해 소규모 중간 단계 임상을 진행한 결과 몰누피라비르 투여 5일 뒤 환자들 모두 양성 반응을 보이지 않았으며, 델타형을 비롯해 각종 변이주에 모두 효과가 있다고 밝혔다.
또 세계 각국 경·중증 환자 775명을 대상으로 진행한 내부 임상 결과 몰누피라비르가 입원·사망률을 약 50% 감소시키는 것으로 나타났다고 발표했다.
미국 정부는 이미 몰누피라비르 승인 시 170만 회분(courses)을 구입하기로 합의했다. 가격은 1회분(course)당 700달러(약 83만원) 수준으로 계약을 맺었다.
태국 정부도 20만 회분, 호주도 30만 회분을 각각 구입 중이며, 한국을 포함해 필리핀과 대만, 말레이시아 등 여러 나라에서 구매를 협의 중인 것으로 전해진다.
김부겸 총리는 최근 한 라디오 방송에서 "2만 명분의 먹는 치료제 선구매 계약을 체결했다"고 밝혔는데, 이 치료제가 몰누피라비르일 가능성이 제기된다.
한편, 이날 FDA 전문가 패널의 머크 논의 일정은 블룸버그통신에서 최초 보도했으며, 이후 로이터가 FDA의 확인을 통해 후속 보도했다.
※ 저작권자 ⓒ 뉴스1코리아, 무단전재-재배포 금지