관련종목▶
전임상까지 진행된 후보물질로 임상시 원치않는 결과땐 개발 중단
단계별 기술료 받아 잃을것 없어.. 작년 5兆 등 해마다 수출 늘어
단계별 기술료 받아 잃을것 없어.. 작년 5兆 등 해마다 수출 늘어
최근 한미약품이 다국적 제약사 릴리에 기술수출한 면역질환 치료제 'BTK 억제제'(프로젝트명 HM71224)의 수출 계약이 해지되면서 기술수출에 대해 관심이 높아지고 있다.
6일 한국제약바이오협회에 따르면 지난 2015년부터 본격화되기 시작한 신약기술 수출을 달성한 국내 제약사만 49개사에 달한다. 또 협회가 국내 제약바이오기업 100곳을 대상으로 진행한 신약 파이프라인 설문조사에 따르면 국내 제약사가 개발 중인 신약은 573개다. 유형별로는 바이오신약이 260개로 가장 많았다. 화학합성신약은 225개, 천연물·개량신약은 88개다.
■기술수출, 신약개발, 디딤돌 역할
한미약품의 기술수출 계약 해지는 이번이 처음이 아니다. 지난 2016년 베링거인겔하임에 내성표적 항암신약 올무티닙(HM61713)에 대한 기술수출 계약이 무산되기도 했다. 한미약품 관계자는 "릴리에서 반환한 후보물질을 독자 개발하는 방안을 검토하기로 했다"고 밝혔다.
다른 수출과 달리 신약개발 과정에서 기술수출 해지는 특별한 일은 아니다. 이는 신약개발 과정의 특수성 때문이다. 일반적으로 하나의 신약을 개발하기 위해서는 평균 15년의 시간과 1조원이 넘는 비용이 든다. 신약 개발은 신약 후보물질을 탐색하는 과정에서 많은 시간과 비용이 들어간다. 이후 쥐, 토끼, 영장류와 같은 동물에 투여해 효능과 부작용을 알아보는 전임상 과정을 거친다. 이 과정에서 유효성과 안전성을 입증해야 사람에게 임상시험을 진행할 수 있다. 총 3번의 임상시험을 거친 후 신약개발이 완성된다.
하지만 이 과정이 쉽지 않다. 미국 바이오협회가 2006년부터 2015년까지 미국 FDA의 9985건의 임상자료를 분석한 결과, 신약 후보 물질이 임상 1상부터 품목승인까지 전 과정을 통과할 확률은 9.6%에 불과했다. 제약사에서는 이 과정을 줄이기 위해 전임상까지 진행된 신약 후보물질을 사들이는 것이다. 하지만 임상시험 과정에서 원하지 않는 결과가 도출되면 개발을 중단하게 된다. 한미약품의 경우 릴리가 임상·개발·허가·상업화에 따른 단계별 기술료(마일스톤)까지 최대 7억6500만달러(약 8600억원)를 지급하기로 합의했다. 이번에 권리를 반환하더라도 한미약품이 이미 수령한 계약금 5300만달러(약 600억원)는 릴리에 돌려주지 않는다. 국내 제약사들이 기술수출을 선택하는 것은 글로벌 시장에서 임상시험을 진행하려면 비용이 많이 들기 때문이다. 또 임상 3상을 진행한 후 신약으로 출시될 확률도 낮기 때문에 리스크를 줄이기 위해서다.
■국내 제약사 기술수출 늘어날 것
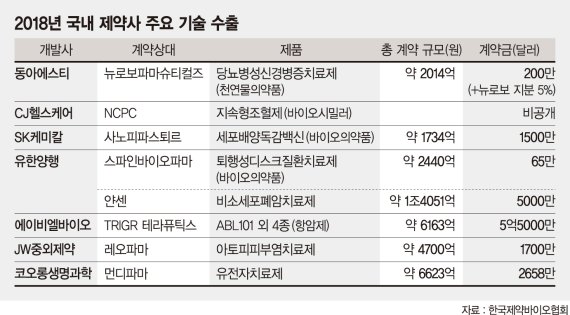
지난해 국내 제약사들의 기술수출이 약 5조원 규모로 전년대비 3배 이상 늘어난 것으로 조사됐다. 한국보건산업진흥원의 해외 기술수출 자료에 따르면 유한양행이 얀센에 비소세포폐암치료제를 약 1조4051억원에 기술수출한 것을 비롯, 12건 약 5조 3706억원 규모에 달했다. 이는 2017년 8건 약 1조 4000억원에 3배에 달하는 것이다.
국내 제약사가 기술수출을 본격적으로 진행한 것은 2015년 한미약품이 미국, 독일, 프랑스, 중국 등에 류마티스관절염 치료제, 폐암 치료제를 비롯해 6건의 기술수출을 진행한 이후다. 2015년에는 한미약품을 비롯, CJ헬스케어, 보령제약, 비씨월드제약, 삼진제약, 일양약품, 제넥신 등 7개사가 기술수출을 진행했다. 약 3조원이 넘는 규모였지만 한미약품의 건당 계약금액이 크기 높은 비중을 차지했다. 하지만 2016년에는 10개사 제약사들이 11건 3조1000억원 규모의 기술수출을 진행했다. 원희목 한국제약바이오협회 회장은 "국내 제약바이오업계가 선도물질부터 임상3상까지 진행중인 합성·바이오 신약 파이프라인이 최소 573개에 달한다"며 "최근 들어 동시다발적으로 터져나오는 신약기술 수출성과가 국내제약산업이 성장을 눈앞에 두고 있다는 것을 확실하게 보여준다"고 강조했다.
pompom@fnnews.com 정명진 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지