삼성바이오에피스, 美 시장 공략
아바스틴 복제약 FDA 허가 대기
셀트리온은 유방암 약 출시 앞둬
내달 류마티스 치료제 獨서 출시
한미약품 자체 개발한 '롤론티스' 4조원대 호중구감소증 시장 노려
아바스틴 복제약 FDA 허가 대기
셀트리온은 유방암 약 출시 앞둬
내달 류마티스 치료제 獨서 출시
한미약품 자체 개발한 '롤론티스' 4조원대 호중구감소증 시장 노려
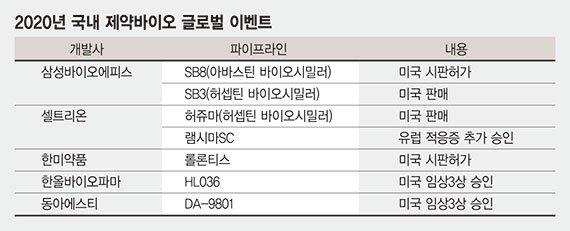
10일 업계에 따르면 올해 제약바이오업계가 기대하고 있는 파이프라인은 삼성바이오에피스의 SB8과 SB3, 셀트리온의 허쥬마, 램시마SC, 한미약품 롤론티스. 한올바이오파마 HL036, 동아에스티 DA-9801 등이다.
삼성바이오에피스는 아바스틴 바이오시밀러(바이오의약품 복제약) SB8이 올해 미 식품의약국(FDA) 시판허가를 받을 것으로 기대하고 있다. 아바스틴은 스위스 제약사 로슈가 판매 중인 항암제로 전이성 대장암, 비소세포폐암 등의 치료에 사용된다.
삼성바이오에피스는 올해 상반기에는 유방암 치료제 허셉틴 바이오시밀러 'SB3' 출시를 계획하고 있다. SB3는 지난해 1월 FDA 시판허가를 받았다.
셀트리온은 미국 시장에서는 허셉틴 바이오시밀러 허쥬마, 유럽에서는 류마티스 관절염 치료제 램시마SC에 대한 기대를 키우고 있다. 셀트리온은 허쥬마를 미국 시장에 올해 1·4분기 내놓을 계획이다.
셀트리온은 독자 개발해 유럽의약품청(EMA) 시판허가를 받은 램시마SC는 다음달 독일에서 출시할 예정이다. 오는 3월에는 영국, 네덜란드에 순차 출시하고 올해 말까지 유럽 전역으로 램시마SC 판매를 확대할 예정이다.
또 램시마SC에 올해 중반기까지 염증성 장질환(IBD), 크론병 등 적응증을 추가해 EMA 승인을 확보할 계획이다. 셀트리온 관계자는 "적응증 추가 승인에 앞서 오는 2월 오스트리아 빈에서 열리는 유럽 크론병 학회(ECCO)에서 임상결과를 발표할 계획이다"고 말했다.
제약업체들도 다양한 파이프라인을 통해 미국 FDA 시판허가 및 임상3상 승인을 기다린다.
한미약품은 지난 연말 자체 개발한 호중구감소증 치료제 '롤론티스'에 대한 FDA의 시판허가를 기대하고 있다. 업계에 따르면 롤론티스에 대한 FDA의 허가 여부는 오는 10월 결정될 것으로 보인다. 롤론티스가 FDA 허가를 획득하면 15년 만에 출시된 호중구감소증 신약이 된다.
호중구감소증은 백혈구 50~70%를 차지하는 호중구가 항암치료 중 비정상적으로 감소해 감염에 취약해지는 병이다. 호중구감소증 치료 시장은 미국서 4조원대 규모를 형성한다.
대웅제약 자회사 한올바이오파마는 올해 1·4분기 안구건조증 치료제 후보물질 'HL036' FDA 임상 3상 주요 결과를 공개한다. 안구건조증은 눈물이 부족하거나 빨리 말라 안구 표면이 손상되는 질환이다. 전세계 4000만명 가량이 안구건조정을 앓고 있고 관련 시장은 세계 3조원 이상으로 평가된다.
동아에스티가 미국 바이오기업 뉴로보파마슈티컬스에 기술수출한 당뇨병성신경병증치료제 'DA-9801' 미국 임상 3상 결과도 올해 발표될 계획이다. 동아에스티는 2018년 1월 뉴로보와 기술이전 계약을 체결했다. 뉴로보 측은 당뇨병성신경통증을 시작으로 DA-9801 적응증을 추가하면서 시장 규모를 키우겠다는 계획이다.
이승규 한국바이오협회 부회장은 "지난해 주요 제약 바이오기업들이 글로벌 임상 3상에서 실패한 사례들이 성장통으로 축적됐다"면서 "이를 보완해 임상과 시판허가 성공률을 높이면 올해 가시적 성과가 나타날 것이다"고 말했다.
junjun@fnnews.com 최용준 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지