질병청 요청, 전문가 의견 등 청취해 긴급사용승인 결정
전문가들 안전성 및 효과성 등 판단 긴급사용 가능 의견
전문가들 안전성 및 효과성 등 판단 긴급사용 가능 의견
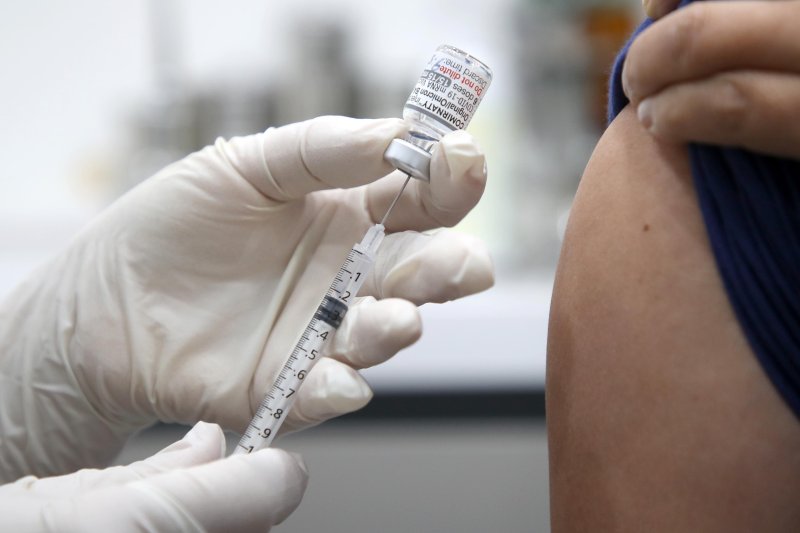
[파이낸셜뉴스] 모더나의 코로나19 오미크론주 BA.4·5 변이 대응 2가백신에 대해 식품의약품안전처는 2일 긴급사용승인을 내렸다. 이번 긴급사용승인은 동절기 코로나19 예방을 위한 오미크론 대응 백신 추가접종 확대 계획에 따라 질병관리청이 이 백신에 대한 도입을 요청하면서 이뤄졌다.
긴급사용승인은 감염병 유행 등 보건 위기 상황에서 관계 중앙행정기관장의 요청이 있는 경우 식약처장이 제조·수입자에게 국내에 허가되지 않은 의료제품을 제조하거나 수입하게 해 공급하는 제도다.
이 백신은 코로나19 초기 바이러스는 물론 변이 바이러스(오미크론주, BA.4와 BA.5 공통부분) 각각의 항원을 발현하는 메신저 리보핵산(mRNA) 2가 백신이다.
사용 대상은 18세 이상 성인이며 기초접종이나 추가접종을 받은 후 최소 3개월 이후 0.5㎖를 추가 접종하는 방식으로 사용된다.
식약처 관계자는 “이번 긴급사용승인 백신은 미국과 유럽에서 긴급사용승인 또는 허가된 백신과 같은 원료의약품을 외국에서 공급받아 국내 삼성바이오로직스에서 충진·표시 등의 공정을 거쳐 완제품으로 생산하는 국내 제조 백신”이라고 말했다.
식약처는 전문가 자문회의를 통해 해당 백신의 감염내과, 약학, 예방의학 등 다양한 분야 전문가(5인)에게 자문했고 전문가들은 신청사가 제출한 자료가 미국과 유럽이 BA.4·5 대응 백신을 검토하기 위해 활용한 자료와 동일하고, 해당 자료에 기반해 긴급사용승인하는 것이 가능하다는 의견을 제시했다.
전문가들은 BA.4·5 대응 2가 백신이 앞서 허가받은 모더나 코로나19 백신과 mRNA 플랫폼, 투여 용량, 제조방식 등이 같은 점을 고려해 해당 백신의 효과성과 안전성이 인정 가능하다는 의견을 냈다. 이후 식약처는 공중보건 위기대응 의료제품 안전관리·공급위원회를 개최해 긴급사용승인을 결정했다.
vrdw88@fnnews.com 강중모 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지